间充质干细胞疗法
2019年4月,波兰科学家Aleksandra Musiał-Wysocka发表在《Cell Transplant》的一篇文章“The Pros and Cons of Mesenchymal Stem Cell-Based Therapies”,论述了间充质干细胞疗法的利弊及发展。可以让大众对于这种方兴未艾的细胞治疗方法有一个初步的了解。文章摘录如下:

概述
各种疾病的新替代疗法研究,促使科学家和医生将注意力集中在再生医学和广为人知的细胞疗法上。目前,干细胞疗法正在被大量的研究,因为它们可能广泛用于许多无法治愈的疾病的治疗。如今,现代治疗策略倾向于使用来自不同来源的间充质干细胞(mesenchymal stem cells,MSCs)。由于其特性,特别是自我再生、分化成几种细胞谱系和参与免疫调节的能力,MSCs已成为制定现代高效治疗策略和临床治疗上的最有希望的工具之一。除了许多优势和好处外,人们还对MSCs的使用存在疑问。MSCs的作用机制是什么?他们如何到达体内?MSCs的临床使用安全吗?这些是MSCs在被视为治疗工具时出现的主要问题。MSCs的多样性、它们不同的临床应用以及它们尚未经过彻底调查的许多特征,是对这些细胞的讨论和有争议的来源。在这里,我们回顾了目前关于MSCs的治疗潜力、临床效果和临床应用安全性方面的知识。
间充质干细胞——细胞治疗的主要参与者
MSCs可以从许多来源中分离出来(图1),它们相对容易体外培养,并且其分化成几种不同细胞类型的能力,以及它们特殊的免疫特性,使MSCs成为细胞治疗和组织再生非常有前景的工具。最知名和最常用的MSCs来源是骨髓(BM)。另一个容易获得的MSCs来源是脂肪组织。从这些来源获取MSCs需要从人体/模式动物中直接获得。有趣的是,MSCs的丰富来源还包括被视为医疗废物的相关组织,如胎盘、脐带、羊水和羊膜。在这些组织中,脐带血就包含MSCs;目前,科学家们还提出了新的MSCs来源。如牙髓、牙周韧带、肌腱、皮肤、肌肉和其他它组织中(图1)。然而,分离效率存在差异,这与供体组织的可用性、状况和年龄有关。一个非常重要的问题是捐赠者细胞的年龄。从年轻捐赠者那里获得的细胞不太容易受到氧化损伤和变化的影响,它们在培养中衰老得慢得多,增殖率更高。
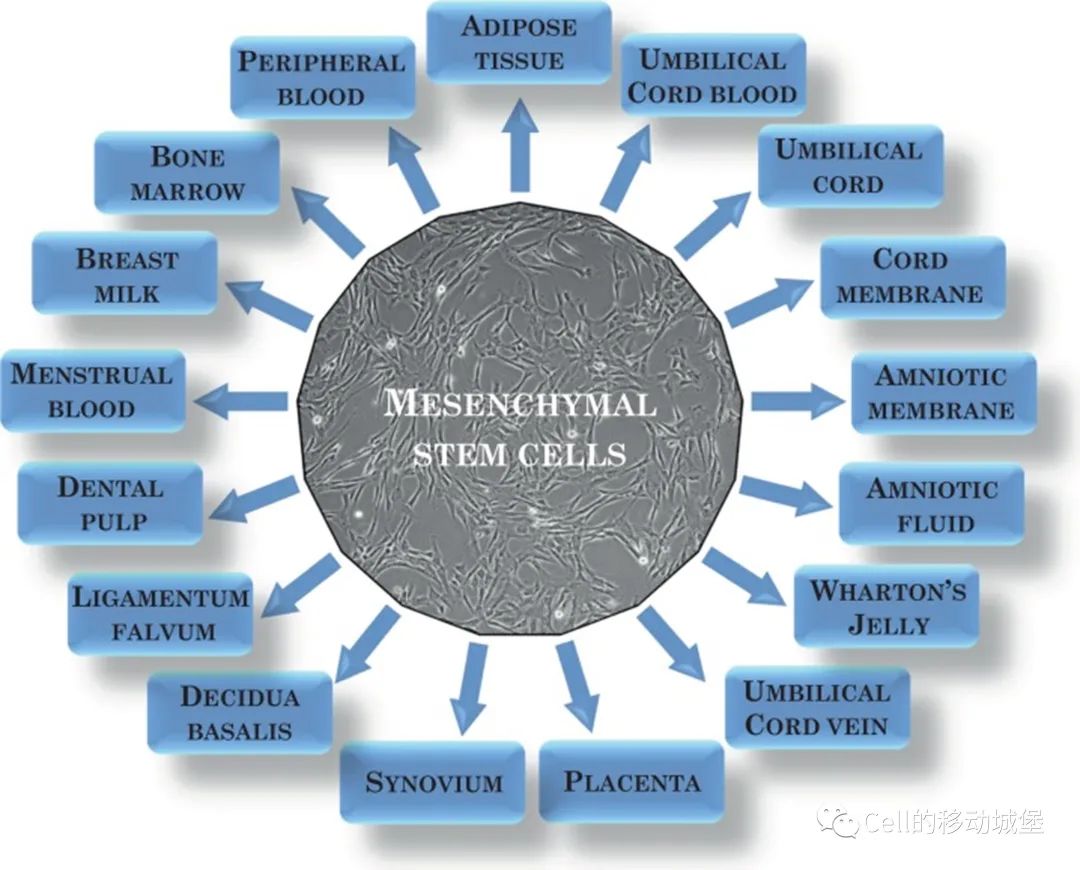
目前,MSCs被用作治疗关节退行性变化以及重建骨骼和软骨的工具,并用于整形手术、美容医学、心血管疾病、内分泌和神经系统疾病、细胞移植和修复受损的肌肉骨骼组织。此外,由于间充质干细胞的特殊特性,例如它们的快速增殖、高分化和迁移到损伤部位的能力,新的临床应用正在测试中。
骨髓间充质干细胞(BM-MSCs)是临床环境中最常用的MSCs。BM-MSCs也首先被美国食品药品监督管理局批准注册为一种名为“Prochymal”的抗移植与宿主疾病的药物。最近,欧洲药品管理局也批准注册了“Alofisel”来治疗perianal fistulas。如今,其它来源的MSCs也在用于临床治疗。
干细胞治疗的新方法是使用细胞外泌体(extracellular vesicles,EV),它可以作为MSCs的替代品。EV从干细胞中释放出来,并向目标部位提供许多成分,如mRNA、DNA和蛋白质。这种方法在最近的许多研究中都有描述,但仍然需要彻底了解其作用机制。
间充质干细胞的迁移和到达
细胞治疗的有效性在很大程度上取决于输送方法。MSCs最常见的给药方法是静脉输液。然而,在细胞到达目标之前,大多数细胞被困在各种器官的毛细血管中,特别是在肺部。这种现象可以解释为MSCs是相对较大的细胞,并表达各种粘附分子。
在某些情况下,动脉内注射似乎是一种更有效的途径。事实证明,与静脉给药相比,通过颈内动脉输送MSCs更能促进其迁移和到达受伤的大脑,这种途径相关的医疗风险包括微血管堵塞。
另外,当MSCs直接输送到受损区域附近的心脏时,到达梗死周围区域的细胞数量要高得多。
间充质干细胞的免疫学特性
人们普遍认为,MSCs没有表现出免疫原性,因此它们可以移植到同种异体宿主,而不会产生受体的免疫反应。它们的作用机制基于免疫调节特性以及免疫抑制活性,能够抑制免疫系统不同细胞的增殖和激活。
间充质干细胞疗法的安全性
到目前为止,已经进行了许多研究来调查基于MSCs的治疗的安全性。
一个加拿大小组分析了使用BM-MSCs的临床试验。在对36项研究进行分析后,他们发现MSCs的使用与受体的致癌反应之间没有关系,也没有报告有严重的副作用。Karussis等人还研究了MSCs治疗在多发性硬化症和肌萎缩侧索硬化症患者中的安全性和影响。在34名接受检查的患者中,在一项持续25个月的研究中,没有观察到治疗产生的严重不利影响。此外,20名患者在移植1年后接受了检查,核磁共振成像结果没有显示任何令人不安的变化。然而,我们仍需要对使用MSCs疗法的安全性进行更多的长期研究和观察。
为了成功应用MSCs,仍有一些问题需要解决。其中之一涉及需要获得足够数量的细胞。但在长期培养期间,MSCs可能会失去了分化的能力,并开始表现出形态变化。更重要的是,MSCs的长期体外培养可能会导致其恶性转化的概率增加。培养基的某些成分和生长因子可能会随着细胞进入受体内。给药后还有病毒和朊病毒传播的风险。
间充质干细胞疗法的黑暗面
在使用干细胞疗法时,应考虑所有可能的不良影响。部分文献讨论了干细胞移植后肿瘤发生的风险。从某种意义上说,干细胞可以与肿瘤细胞比较类似,因为它们都能够长期增殖,具有很高的生存能力,并且对受体的细胞凋亡机能有抵抗力。许多成分可能会影响MSCs移植后的潜在肿瘤发生,包括供体年龄、宿主组织、受体组织表达的生长调节剂,以及控制MSCs在目标部位行为的机制。此外,MSCs的操作和长期体外培养可能导致遗传不稳定和染色体异常。这些累积因素可以以自发肿瘤转化的形式做出表现。干细胞移植患者通常接受长期化疗或放疗,因此他们的免疫系统无法正常工作,这可能也与肿瘤发生的风险有关。
间充质干细胞疗法的光明面
MSCs在致瘤性方面表现出二元性。一些研究显示了它们的抗肿瘤作用。MSCs分泌的因素可能具有抗肿瘤特性。Clarke等人表明,与在标准培养基中培养的细胞相比,在MSCs条件培养基中培养的乳腺癌细胞表现出显著的迁移抑制作用。MSCs的肿瘤发生效应可以通过分泌蛋白质TIMP-1和TIMP-2来发挥,这些蛋白质会抑制参与肿瘤迁移过程的MMPs的活性。
Bruno等人还研究了MSCs对肿瘤细胞生长的抑制作用。从MSCs中分离出来的微泡(microvesicles,MV)通过抑制细胞周期进展和诱导肿瘤细胞凋亡和坏死,导致肿瘤细胞增殖显著减少。这些观察结果得到了体内研究的证实,减缓了肿瘤的生长速度。
关于MSCs在肿瘤治疗中的潜力,目前并没有明确的答案。事实上,MSCs的影响不仅取决于所使用的肿瘤模型,还取决于培养方法、细胞异质性、剂量、分泌物以及许多其它尚未完全了解的因素。
与间充质干细胞应用相关的其他限制
大多数研究表明,一次MSCs移植是安全的,不会诱发免疫反应。然而,反复注射MSCs可能会导致同种异体免疫反应的产生。此外,MSCs培养基中使用的胎牛血清(FBS)可能会对接受此类细胞的患者产生免疫反应。Von Bonin等人表明,与FBS接触的MSCs的移植诱导了受体血液中FBS抗体的产生。
写在最后
干细胞无疑是治疗许多疾病的一大希望。由于它们存在于许多成人组织中,并且不会引起伦理问题,因此与胚胎干细胞相比,它们具有巨大优势。由于它们的独特特征,例如易于分离和培养,在许多组织中的可用性,免疫调节特性,我们认为它们可用于自体和同种异体的移植。尽管进行了大量体外和体内研究,但MSCs迁移和到达背后的机制需要进一步详细研究。然而,毫无疑问,这些细胞可以迁移并进入受伤的组织。关于MSCs治疗的潜在长期风险,正在做更多研究。我们需要进行长期研究和观察,以调查MSCs疗法的长期影响,包括负面影响。根据我们的数据,间充质干细胞疗法的使用是再生医学中很有前途的工具。
转自公众号:Cell的移动城堡
上一篇:类器官的发展历史
下一篇:

 在线咨询
在线咨询 